使用 SQK-RPB114.24 进行细菌、真菌和病毒病原体监测的快速宏基因组测序 (RMS_9215_v114_revF_18Nov2025)
MinION: Protocol
使用 SQK-RPB114.24 进行细菌、真菌和病毒病原体监测的快速宏基因组测序 V RMS_9215_v114_revF_18Nov2025
本实验指南提供了一种快速的宏基因组测序方法,用于鉴定细菌、真菌和病毒性病原体。
此指南具有以下特点:
- 采用二合一流程,可将同一样品分别进行细菌/真菌与病毒/非细胞前处理;
- 提供针对呼吸道样品的宿主去除与核酸提取方法;
- 采用 RT-PCR “鸟枪法”策略;
- 包含酶切法片段化、条形码标记及 PCR 扩增步骤;
- 适用于 R10.4.1 测序芯片。
仅供研究使用
FOR RESEARCH USE ONLY.
概览
本实验指南提供了一种快速的宏基因组测序方法,用于鉴定细菌、真菌和病毒性病原体。
此指南具有以下特点:
- 采用二合一流程,可将同一样品分别进行细菌/真菌与病毒/非细胞前处理;
- 提供针对呼吸道样品的宿主去除与核酸提取方法;
- 采用 RT-PCR “鸟枪法”策略;
- 包含酶切法片段化、条形码标记及 PCR 扩增步骤;
- 适用于 R10.4.1 测序芯片。
仅供研究使用
1. 实验方案概览
本品为早期试用产品。
如需有关早期试用计划的更多信息,请参阅 本文了解产品的不同发布阶段。
请确保始终使用最新版本的实验指南。
快速宏基因组测序实验指南简介
本指南介绍了一种针对提取的样品核酸进行非靶向宏基因组测序的方法。
该方法根据目标样品类型和起始材料,提供了两种制备方案:
- 细菌/真菌样品(针对DNA):使用 SQK-RPB114.24 试剂对样本中提取的全部 DNA 进行片段化(tagmentation),继而进行扩增与测序。
- 病毒样品(DNA 和 RNA):该方法由 Oxford Nanopore Technologies 在 Josh Quick 与 Ingra M. Claro 建立的流程基础上优化,采用鸟枪法测序策略,使用 9N 引物随机逆转录 RNA,并对样品中所有 DNA 和 RNA 进行 PCR 扩增。
补充说明:
- 该方法已针对呼吸道样品优化,其表现受样品类型影响;
- 样品复杂度低、核酸背景少时,检测效果更佳。
本实验指南使用快速扩增条码试剂盒 V14(SQK-RPB114.24),单次测序实验可支持多达 24 种条形码。
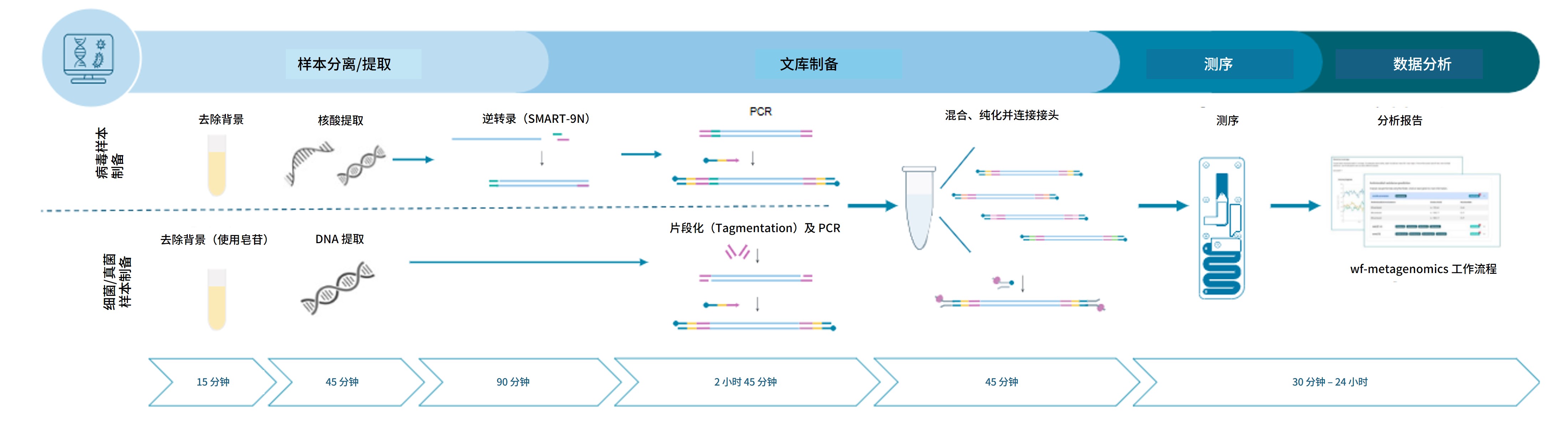
更多信息及示例数据,请参阅我们的使用 SQK-RPB114.24 进行细菌、真菌和病毒病原体监测的快速宏基因组测序专题技术文档。
测序工作流程:
实验准备
您将需要:
- 确保已准备好测序试剂盒、正确的仪器以及第三方试剂
- 若未采用本方案的呼吸道样品处理流程,请先完成 DNA/RNA 提取
- 下载数据收集和分析软件
- 检查测序芯片上有足够的活性纳米孔,以确保测序良好运行
宿主去除与核酸提取
- 若您采用我们推荐的呼吸道样品宿主去除与提取流程,请确保已备齐所需的第三方试剂
- 请使用新鲜样品,避免选用冷冻或灭活样品
文库制备
下表概述了文库制备所需的步骤,包括时间安排和可以中止的节点。
| 实验步骤 | 流程 | 时间 | 中止节点 |
|---|---|---|---|
| 病毒样品:逆转录 | 使用 RLB RT 9N 引物混合液 与 TSOmG 模板转换寡核苷酸对 RNA 样品进行逆转录 | ~90 分钟 | |
| 细菌/真菌样品:DNA 酶切法片段化 | 使用测序试剂盒提供的片段化反应试剂酶切 DNA 样本 | 10 分钟 | |
| PCR 扩增 | 使用测序试剂盒提供的带条形码引物对样品进行 PCR 扩增 | 180 分钟 | 非必需: PCR 扩增完成后,可在保温温度下继续放置过夜。 |
| 样品定量及混合 | 对带条形码的 PCR 样品进行定量,并按等摩尔比例混合 | 15 分钟 | |
| 纯化与定量 | 纯化合并后的样品并重新定量 | 15 分钟 | 4°C 过夜 |
| 快速测序文库接头连接与纯化 | 将测序接头连接至 DNA 末端 | 5 分钟 | 我们强烈建议在连接测序接头后即对文库进行测序。 |
| 测序芯片的预处理及上样 | 对测序芯片进行预处理,然后将制备好的文库加至芯片中进行测序 | 10 分钟 |
测序和分析
您将需要:
- 使用 MinKNOW 软件开始测序。该软件会通过测序仪收集原始数据,并将其识别成碱基序列
- 通过 EPI2ME 平台或命令行,使用 wf-metagenomics workflow 工作流程对数据进行分析。
实验方案适用性
本实验方案只适用于与以下产品搭配使用:
- 快速PCR条形码测序试剂盒(SQK-RPB114.24)
- 测序芯片清洗剂盒(EXP-WSH004)
- R10.4.1 测序芯片(FLO-MIN114)
- 快速测序文库接头辅助扩展包 V14 (EXP-RAA114)
- 测序辅助扩展包 V14 (EXP-AUX003)
- 测序芯片预处理试剂盒 (EXP-FLP004)
- MinION Mk1D - MinION Mk1D IT 配置要求文档
- GridION - GridION IT 配置要求文档
2. 实验器材及耗材
材料
- (用于样品制备)细菌/真菌或病毒/非细胞起始样品(详见下文)
- (用于文库制备)经提取的核酸
- 快速 PCR 条形码测序试剂盒-24 V14(SQK-RPB114.24)
耗材
- MinION/GridION 测序芯片
- Sputasol(Fisher,11943262)
- RT-PCR 级水(Fisher,10289774)
- 磷酸盐缓冲液(PBS)(Fisher, 11593377)
- 2X HL-SAN 缓冲液(含 4.5 M NaCl 和 100 mM MgCl₂),由以下两种试剂配制:
- Invitrogen 5M NaCl(Fisher,10255984)
- Invitrogen 1M MgCl2(Fisher,10418464)
- HL-SAN 无 Triton 核酸酶(ArcticZymes,70911-202)
- 皂苷溶液(0.2% 皂苷,溶于 PBS),由以下试剂配制:
- 皂苷(Sigma-Aldrich, 47036-50G-F)
- 裂解介质 E 管(Fisher, 11452420)
- MagMAX 病毒/病原体核酸提取试剂盒(Fisher,16346582)
- 12 µM RLB RT 9N 引物(IDT - 序列:5’-TTTTTCGTGCGCCGCTTCAACNNNNNNNNN-3’)
- 12 µM TSOmG 模板转换寡核苷酸(IDT - 序列:5’-GCTAATCATTGCTTTTTCGTGCGCCGCTTCAACATmGmGmG-3’)
- 10 mM dNTPs(Fisher,10610851)
- Maxima H Minus 逆转录酶(Fisher,13233159)
- RNaseOUT(Fisher,10777019)
- LongAmp 热启动 Taq 酶 2X 预混液(NEB, M0533)
- Thermolabile 核酸外切酶 I(NEB, M0568)
- Agencourt AMPure XP 磁珠(Beckman Coulter™, A63881)
- 无核酸酶水(如 Thermo Scientific,AM9937)
- 牛血清白蛋白(BSA)(50 mg/mL)(例如 Invitrogen™ UltraPure™ BSA 50 mg/mL, AM2616)
- 1.5 ml Eppendorf DNA LoBind 离心管
- 0.2 ml 薄壁PCR管
- Qubit™ dsDNA HS Assay(双链 DNA 高灵敏度检测)试剂盒(ThermoFisher,Q32851)
- Qubit™ 分析管(Invitrogen, Q32856)
仪器
- MinION 或 GridION 测序仪
- MinION/GridION 测序芯片遮光片
- 台式微量离心机(最高转速 15000 rpm)
- 迷你离心机
- 计时器
- 涡旋混匀仪
- 设定为 37 °C 的恒温混匀仪
- 设定为 65 °C 的恒温混匀仪
- 磁力架
- 株磨匀浆仪(例如 FastPrep-24™ Classic 珠磨匀浆与裂解系统)
- 热循环仪
- 96 孔 PCR 反应模块
- 盛有冰的冰桶
- Hula混匀仪(低速旋转式混匀仪)
- Qubit荧光计 (或用于质控检测的等效仪器)
- P1000 移液枪和枪头
- P200 移液枪和枪头
- P100 移液枪和枪头
- P20 移液枪和枪头
- P10 移液枪和枪头
- P2 移液枪和枪头
可选仪器
- 与样品相匹配的生物安全防护设备(如在符合 BSL-3 要求的实验室环境下,使用Ⅱ级微生物安全柜或同等设备)
请在符合相应生物安全条件的环境中处理病原性样品。
请严格遵守实验室规范及本地相关法规的健康与安全要求。
注意: 我们建议您至少在 II 级生物安全柜内进行操作。请注意,部分微生物在研磨珠裂解步骤中仍可能存活。请在样品制备和文库制备过程中采取必要的防护措施。
本实验指南所需起始样本量如下:
样品制备阶段:
- ≥ 250 µl 痰液/气管插管吸取液
或
- ≥ 250 µl 支气管肺泡灌洗液(BAL)/小量 BAL(Mini-BAL)
或
- ≥ 500 µl 于VTM 或 UTM 中保存的口/鼻拭子(仅适用于病毒样品)
注意: 若样品量充足,可同时进行细菌/真菌和病毒的样本制备。但两种处理方法不同,应视为两个独立样品分别操作。
文库制备阶段:
- 从上述样本类型中提取的核酸
起始 DNA/RNA
DNA/RNA 质控
选择符合质量和浓度要求的起始 DNA/RNA 至关重要。使用过少或过多或者质量较差的 DNA/RNA(如,高度碎片化、含有RNA或化学污染物的DNA)均会影响文库制备。
有关如何对 DNA/RNA 样品进行质控,请参考起始DNA/RNA质控实验指南。
化学污染物
从原始样本中提取 DNA/RNA 的方法不同,可能会导致经纯化的 DNA/RNA 中所残留的化学污染物不同。这会影响文库的制备效率和测序质量。请参阅牛津纳米孔社区的污染物 页面了解更多信息。
流程对照
阴性内部对照
为监测潜在污染,我们建议您在整个流程中纳入阴性对照,并按与真实样品相同的方式处理。
您可采用 PBS 或由第三方提供的阴性样本溶液作为阴性对照。
第三方试剂
Oxford Nanopore Technologies 推荐您使用本实验指南中列出的所有第三方试剂,并已对其进行验证。我们尚未对其它替代试剂进行测试。
我们建议您按制造商说明准备待用的第三方试剂。
Agencourt AMPure XP 磁珠
PCR 扩增后的纯化步骤中,除试剂盒提供的 AMPure XP 磁珠(AXP)外,您可能需要额外准备 Agencourt AMPure XP 磁珠。
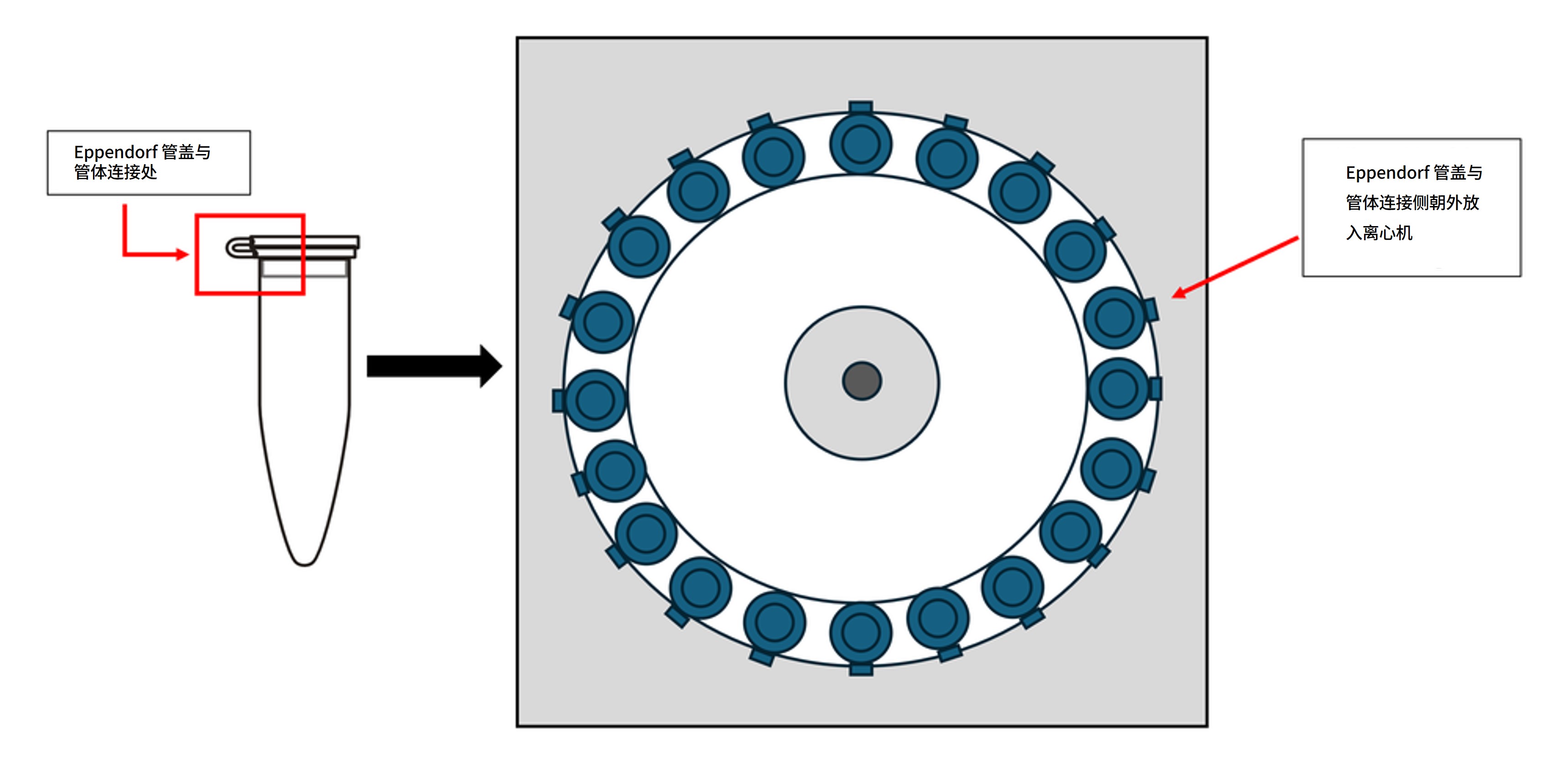
Eppendorf 离心管的放置方向
在所有离心步骤中,请将离心管的管盖与管体连接侧统一朝向外侧放置,以便快速定位沉淀。
取出离心管时应轻拿轻放,避免扰动沉淀。
测序芯片质检
我们强烈建议您在开始测序实验前,对测序芯片的活性纳米孔数进行质检。质检需在您收到 MinION/GridION 测序芯片12周内进行。Oxford Nanopore Technologies会对活性孔数量少于以下标准的芯片进行替换*:请您按照测序芯片质检文档中的说明进行芯片质检。
| 测序芯片 | 芯片上的活性孔数确保不少于 |
|---|---|
| MinION/GridION 测序芯片 | 800 |
*(请注意:自收到之日起,芯片须一直贮存于Oxford Nanopore Technologies推荐的条件下。且质检结果须在质检后的两天内递交给我们。)
本试剂盒及其实验指南中使用的快速测序文库接头(RA)不可与其他测序接头互换使用。
快速PCR条形码测序试剂盒-24 V14 (SQK-RPB114.24)内容物
我们正在将试剂盒中的快速条形码引物包装更改为96孔板形式。同时,孔板形式的快速条形码引物浓度已由原瓶装形式的 10 µM 降低至 1 µM。这一改动将减少塑料浪费,并支持自动化应用。
请务必根据试剂盒的包装形式和快速条形码引物的浓度,严格按照相应说明进行操作。
以孔板形式提供的 1 µM 浓度快速条形码引物
| 名称 | 缩写 | 管数 | 管盖颜色 | 每管溶液体积 (μl) |
|---|---|---|---|---|
| 片段化反应试剂 | FRM | 1 | 棕色 | 160 |
| 快速测序文库接头 | RAP | 1 | 绿色 | 15 |
| 接头缓冲液 | ADB | 1 | 透明 | 100 |
| AMPure XP 磁珠 | AXP | 3 | 琥珀色 | 1,200 |
| 洗脱缓冲液 | EB | 2 | 黑色 | 500 |
| EDTA | EDTA | 1 | 蓝色 | 700 |
| 测序缓冲液 | SB | 1 | 红色 | 700 |
| 文库颗粒 | LIB | 1 | 粉色 | 600 |
| 文库溶液 | LIS | 1 | 白色管盖,粉色标签 | 600 |
| 测序芯片冲洗液 | FCF | 1 | 透明管盖,浅蓝色标签 | 8,000 |
| 测序芯片系绳 | FCT | 1 | 紫色 | 200 |
| 浓度为 1 µM 的快速条形码引物 (01-24) | RPB | - | 两板,每板三套条形码引物组合 | 每孔 15 µl |
注意: 本产品包含由贝克曼库尔特公司(Beckman Coulter, Inc)生产的 AMPure XP 试剂,并可与试剂盒一起于-20°C 下储存(试剂稳定性将不受损害)。
以管装形式提供的 10 µM 浓度快速条形码引物
| 名称 | 缩写 | 管数 | 管盖颜色 | 每管溶液体积 (μl) |
|---|---|---|---|---|
| 浓度为 10 µM 的快速条形码引物 | RLB01-24 | 24(每管含一种条形码) | 透明 | 15 |
| 片段化反应试剂 | FRM | 1 | 棕色 | 160 |
| 快速测序文库接头 | RAP | 1 | 绿色 | 15 |
| 接头缓冲液 | ADB | 1 | 透明 | 100 |
| AMPure XP 磁珠 | AXP | 3 | 琥珀色 | 1,200 |
| 洗脱缓冲液 | EB | 2 | 黑色 | 500 |
| EDTA | EDTA | 1 | 蓝色 | 700 |
| 测序缓冲液 | SB | 1 | 红色 | 700 |
| 文库颗粒 | LIB | 1 | 粉色 | 600 |
| 文库溶液 | LIS | 1 | 白色管盖,粉色标签 | 600 |
| 测序芯片冲洗液 | FCF | 1 | 白色 | 8,000 |
| 测序芯片系绳 | FCT | 1 | 紫色 | 200 |
注意: 本产品包含由贝克曼库尔特公司(Beckman Coulter, Inc)生产的 AMPure XP 试剂,并可与试剂盒一起于-20°C 下储存(试剂稳定性将不受损害)。
快速条形码引物
| 组成 | 序列 |
|---|---|
| 快速条形码引物 01 | AAGAAAGTTGTCGGTGTCTTTGTG |
| 快速条形码引物 02 | TCGATTCCGTTTGTAGTCGTCTGT |
| 快速条形码引物 03 | GAGTCTTGTGTCCCAGTTACCAGG |
| 快速条形码引物 04 | TTCGGATTCTATCGTGTTTCCCTA |
| 快速条形码引物 05 | CTTGTCCAGGGTTTGTGTAACCTT |
| 快速条形码引物 06 | TTCTCGCAAAGGCAGAAAGTAGTC |
| 快速条形码引物 07 | GTGTTACCGTGGGAATGAATCCTT |
| 快速条形码引物 08 | TTCAGGGAACAAACCAAGTTACGT |
| 快速条形码引物 09 | AACTAGGCACAGCGAGTCTTGGTT |
| 快速条形码引物 10 | AAGCGTTGAAACCTTTGTCCTCTC |
| 快速条形码引物 11 | GTTTCATCTATCGGAGGGAATGGA |
| 快速条形码引物 12 | GTTGAGTTACAAAGCACCGATCAG |
| 快速条形码引物 13 | AGAACGACTTCCATACTCGTGTGA |
| 快速条形码引物 14 | AACGAGTCTCTTGGGACCCATAGA |
| 快速条形码引物 15 | AGGTCTACCTCGCTAACACCACTG |
| 快速条形码引物 16 | CGTCAACTGACAGTGGTTCGTACT |
| 快速条形码引物 17 | ACCCTCCAGGAAAGTACCTCTGAT |
| 快速条形码引物 18 | CCAAACCCAACAACCTAGATAGGC |
| 快速条形码引物 19 | GTTCCTCGTGCAGTGTCAAGAGAT |
| 快速条形码引物 20 | TTGCGTCCTGTTACGAGAACTCAT |
| 快速条形码引物 21 | GAGCCTCTCATTGTCCGTTCTCTA |
| 快速条形码引物 22 | ACCACTGCCATGTATCAAAGTACG |
| 快速条形码引物 23 | CTTACTACCCAGTGAACCTCCTCG |
| 快速条形码引物 24 | GCATAGTTCTGCATGATGGGTTAG |
3. 宿主去除与样本提取
材料
- 痰液/气管插管吸取液
- 支气管肺泡灌洗液(BAL)/小量 BAL(Mini-BAL)
- 于VTM 或 UTM 中保存的口/鼻拭子(仅适用于病毒样品)
耗材
- Sputasol(Fisher,11943262)
- RT-PCR 级水(Fisher,10289774)
- 磷酸盐缓冲液(PBS)(Fisher, 11593377)
- 2X HL-SAN 缓冲液(含 4.5 M NaCl 和 100 mM MgCl₂),由以下两种试剂配制:
- Invitrogen 5M NaCl(Fisher,10255984)
- Invitrogen 1M MgCl2(Fisher,10418464)
- HL-SAN 无 Triton 核酸酶(ArcticZymes,70911-202)
- 皂苷溶液(0.2% 皂苷,溶于 PBS),由以下试剂配制:
- 皂苷(Sigma-Aldrich, 47036-50G-F)
- 裂解介质 E 管(Fisher, 11452420)
- MagMAX 病毒/病原体核酸提取试剂盒(Fisher,16346582)
- 1.5 ml Eppendorf DNA LoBind 离心管
- 15 ml Falcon离心管
仪器
- 台式微量离心机(最高转速 15000 rpm)
- 迷你离心机
- 计时器
- 涡旋混匀仪
- 设定为 37 °C 的恒温混匀仪
- 设定为 65 °C 的恒温混匀仪
- 磁力架
- 株磨匀浆仪(例如 FastPrep-24™ Classic 珠磨匀浆与裂解系统)
- P1000 移液枪和枪头
- P200 移液枪和枪头
- P20 移液枪和枪头
- P10 移液枪和枪头
可选仪器
- 与样品相匹配的生物安全防护设备(如在符合 BSL-3 要求的实验室环境下,使用Ⅱ级微生物安全柜或同等设备)
请确保将细菌/真菌样本与病毒样本分开处理。
为避免混用或误用制备方法,处理 细菌/真菌样品 与 病毒样品 时应分开操作。
在文库构建前,如需同时处理不同类型样品,可在保持样品严格分离的前提下并行开展两种制备流程。请根据各样本类型遵循对应的制备流程。
注意: 同一样本可分别用于细菌/真菌与病毒的制备流程。请按照以下说明操作:将上清液用于病毒样本制备,沉淀部分用于细菌/真菌样本制备。请注意,二者的制备方法不同,应视为两个独立样本分别处理。
请确保起始样本量充足。您将需要:
- 250 µl 痰液、气管插管吸出物或其他黏稠样本(如粘液性支气管肺泡灌洗液);
或
- 500 µl 采集于保存液中的拭子样本(或其他液体样本)。
流程对照
阴性内部对照
为监测潜在污染,我们建议您在整个流程中纳入阴性对照,并按与真实样品相同的方式处理。
您可采用 PBS 或由第三方提供的阴性样本溶液作为阴性对照。
使用无核酸酶水,配制 Sputasol 工作液(1:13.33):
- 向一支洁净的 15 ml Falcon 管内加入 750 µl Sputasol。
- 加入 9.25 ml 无核酸酶水。
- 涡旋振荡以充分混匀。
* 可根据实验需求按比例调整配制体积。
配制 0.2% Saponin-PBS 溶液:
| 试剂 | 体积 / 重量 |
|---|---|
| Saponin(Sigma-Aldrich, 47036-50G-F) | 0.01 g |
| PBS 缓冲液(PBS) | 5,000 µl |
| 0.2% Saponin-PBS 溶液总量 | 5,000 µl |
* 可根据实验需求按比例调整配制体积。
0.2% Saponin-PBS 溶液可于 ~4°C 冷藏保存 30 天。
配制 2X HLSAN 缓冲液(含 4.5 M NaCl 和 100 mM MgCl₂):
| 试剂 | 体积 |
|---|---|
| Invitrogen 5M NaCl | 4,500 µl |
| Invitrogen 1M MgCl2 | 500 µl |
| 总体积 | 5,000 µl |
* 可根据实验需求按比例调整配制体积。
配制好的 2X HLSAN 缓冲液可在室温(约 22°C)条件下长期保存。
请将恒温混匀仪分别设定为 37°C 和 65°C。
制备粘液样本(如痰液、气管抽吸物等):
注意: 对于保存在运输保存液中的样本,以及支气管肺泡灌洗液(BAL)样本,一般无需执行此步骤,除非样本呈黏液状。
- 向样本中加入等体积的(1:1)Sputasol 工作液。
- 涡旋振荡混匀 30 秒。
- 室温孵育,直至样本液化(至少 5 分钟)。
提示: 若 5 分钟后样本仍较黏稠,可重复以上操作。痰液充分液化是实现高效宿主去除和核酸提取的关键。
各样本取 500 µl,分别转移至对应的洁净 1.5 ml Eppendorf 离心管中。
10,000 × g 离心 5 分钟。
小心取出离心管,避免扰动管内溶液。
请注意,同一样品可分别用于病毒样品制备和细菌/真菌样品制备。
请按照以下步骤进行操作;若同一样品分别使用不同的制备方法,应将其视为两个独立样品处理。
根据样品类型,可并行进行相应的制备步骤:
| 步骤 | 病毒样本 | 细菌/真菌样本 |
|---|---|---|
| 1. | 对每个样本,吸取 300 µl 上清液(自样本上层),转入一支新的 1.5 ml Eppendorf 管中。 | 可选项: 处理病毒样本后,剩余的沉淀及上清液可用于细菌/真菌样本制备。具体方法如下。 |
| 2. | 使用移液枪小心移除大部分上清液,避免扰动沉淀,保留少量上清覆盖沉淀。 注意: 请确保保留约 50 µl 上清液覆盖沉淀,并避免扰动沉淀。 | |
| 3. | 将沉淀充分重悬于 200 µl 预配的 0.2% saponin-PBS 溶液中。吹打混匀。 | |
| 4. | 向样本上清液中加入宿主去除试剂: • 加入 10 µl HLSAN 酶。 • 涡旋混匀 3 秒。 | 按照以下步骤向重悬沉淀中加入宿主去除试剂: • 加入 200 µl 预配的 2X HLSAN 缓冲液。 • 加入 10 µl HLSAN 酶。 • 涡旋混匀 3 秒。 |
| 5. | 在恒温混匀仪中以 37 °C、1,000 rpm 孵育 10 分钟。 | 在恒温混匀仪中以 37 °C、1,000 rpm 孵育 10 分钟。 |
| 6. | 在各支含有样品上清液的离心管中按下表配制反应体系: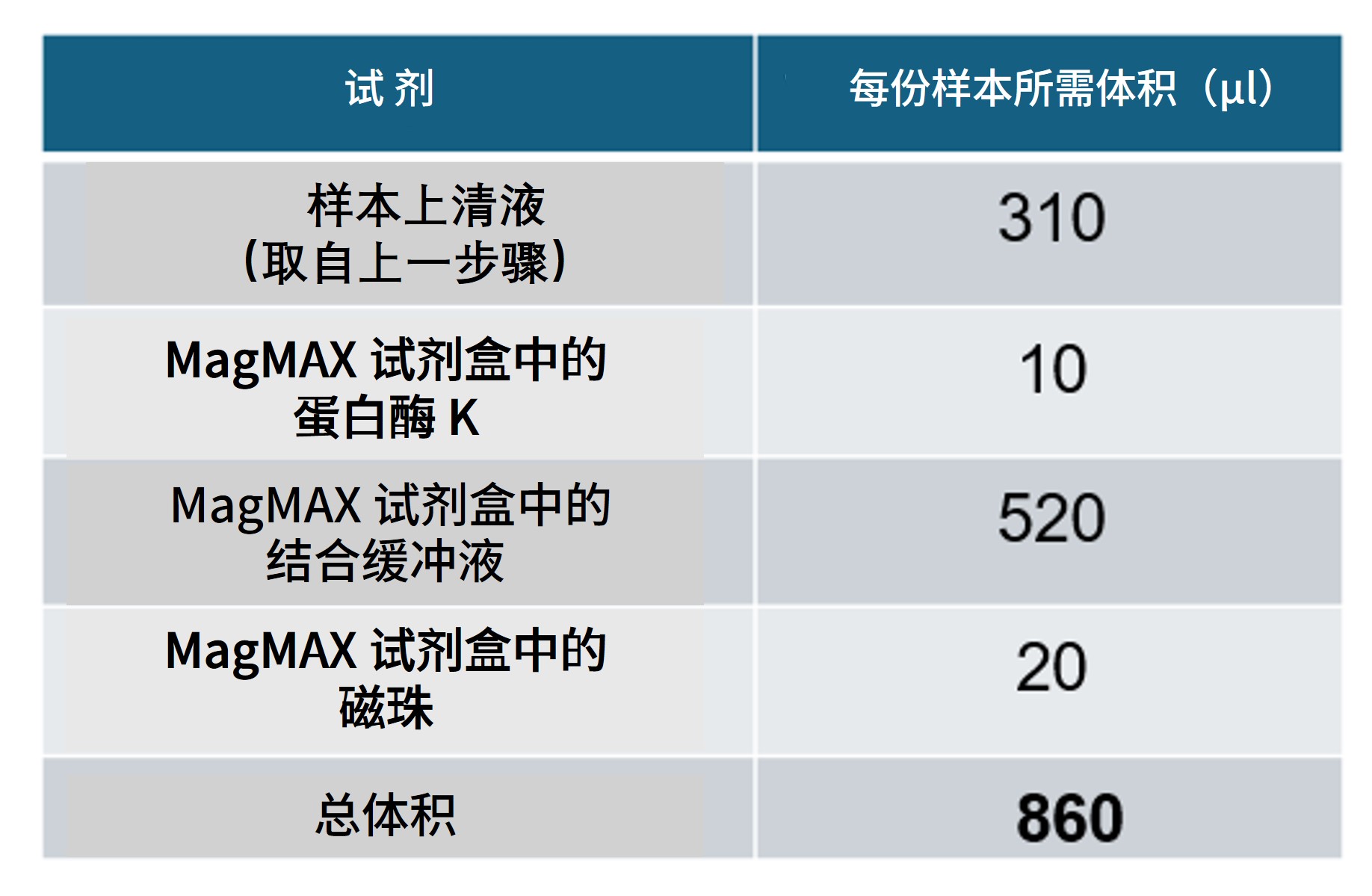 倒转离心管多次以混匀。 避免 剧烈混合裂解试剂或采用可能产生泡沫的方法(如涡旋振荡)。 注意: 您也可提前配制提取试剂预混液,并一次性加入样品上清。 | |
| 7. | 向样本中加入 900 µl PBS,吹打混匀。 | |
| 8. | 以 12,000 × g 离心 3 分钟。 | |
| 9. | 使用移液枪小心移除大部分上清液,避免扰动沉淀,保留少量上清覆盖沉淀。 请确保保留约 50 µl 上清液覆盖沉淀,并避免扰动沉淀。 | |
| 10. | 向沉淀中加入 500 µl PBS,吹打混匀。 | |
| 11. | 将每个样品的全部液体分别转移至独立的研磨珠裂解管(裂解介质 E 管)中。 | |
| 12. | 将研磨珠裂解管置于 FastPrep-24 Classic 珠磨匀浆与裂解系统中,并运行以下程序: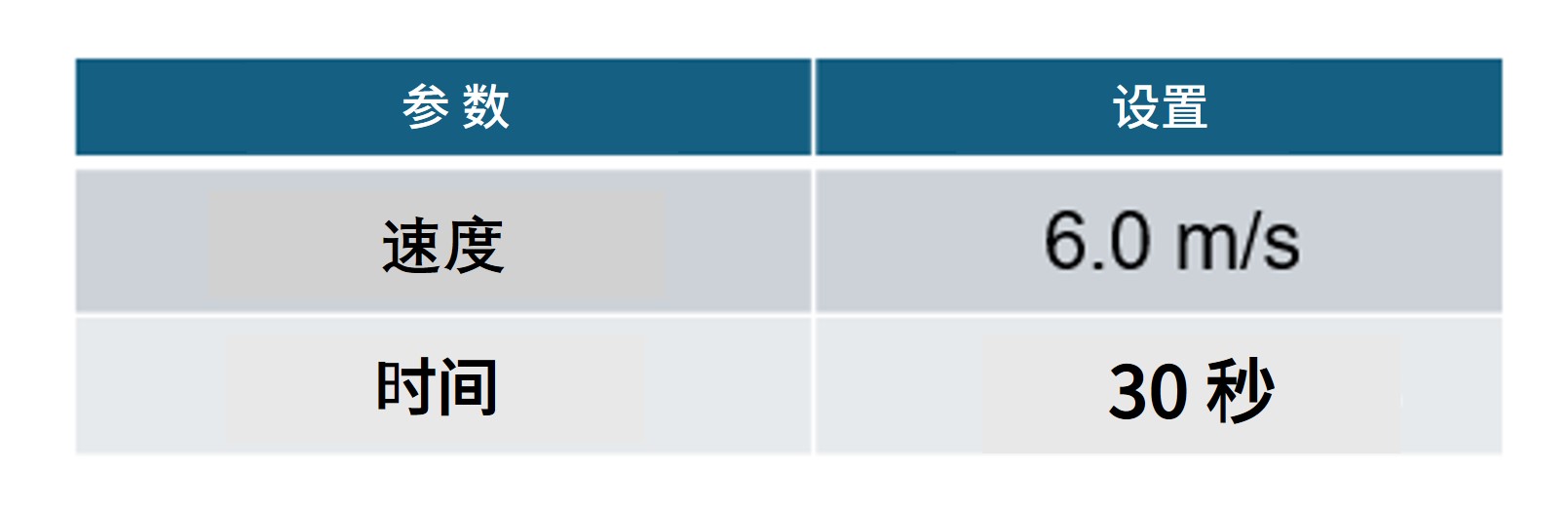 | |
| 13. | 将研磨珠裂解管从 FastPrep 匀浆仪中取出,并在最高转速(>20,000 × g)下离心 30 秒。 | |
| 14. | 每个样品取 300 µl 上清,分别转移至新的 1.5 ml Eppendorf 管中。 注意 :操作时请避免将研磨珠裂解管内的研磨珠一同吸出。 | |
| 15. | 向每管样本上清中加入以下反应体系: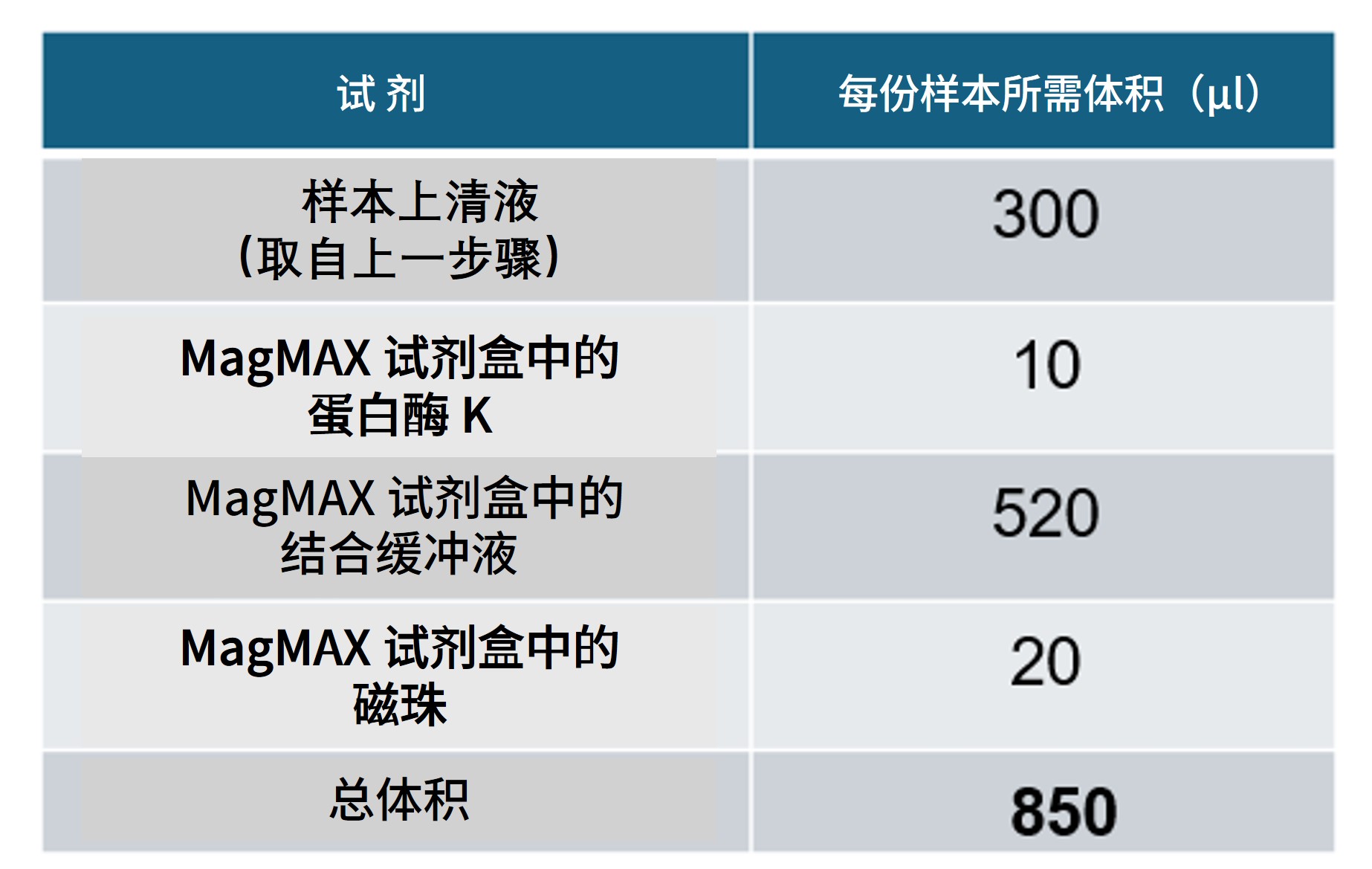 轻轻颠倒离心管数次以混匀。 避免 剧烈混合裂解试剂或采用可能产生泡沫的方法(如涡旋振荡)。 注意: 您也可提前配制提取试剂预混液,并一次性加入样品上清。 |
将所有样品管置于恒温混匀仪中,于 65 °C、1,000 rpm 条件下孵育 5 分钟。
将样本管转移至 Hula 混匀仪,在室温下孵育并混合 5 分钟。
Hula 混匀仪 :
- 轨道旋转 15 rpm(10 秒)
- 往复旋转 70°(15 秒)
- 振动/暂停 5°(3 秒)
- 总时长:5 分钟
注意: 在孵育过程中请务必反复倒转离心管,以避免磁珠沉积于管底。我们强烈建议您使用 Hula 混匀仪;若无此设备,请在孵育期间手动倒转样品管。
为每个样本准备2 ml 新鲜制备的80%乙醇(用无核酸酶水配制)。
将样本瞬时离心后置于磁力架上,待磁珠与液相完全分离,且液相澄清无色(≥ 5 分钟)。保持离心管在磁力架上不动,用移液枪吸去清液。
请小心不要扰动磁珠。
将离心管从磁力架上取下,向其中加入 1 ml MagMAX 试剂盒提供的洗涤缓冲液(Wash Buffer),轻轻倒转离心管直至样品完全重悬。
注意: 请避免使用会产生泡沫的混匀方式,以免影响样品回收率。
将样本瞬时离心后置于磁力架上,待磁珠与液相完全分离,且液相澄清无色(≥ 两分钟)。保持离心管在磁力架上不动,用移液枪吸去清液。
将离心管从磁力架上移开,向管中加入 1 ml 80% 的乙醇。轻轻倒转离心管直至样品完全重悬。
将样本瞬时离心后置于磁力架上,待磁珠与液相完全分离,且液相澄清无色(≥ 两分钟)。保持离心管在磁力架上不动,用移液枪吸去清液。
将离心管从磁力架上移开,向管中加入 500 µl 80% 的乙醇。轻轻倒转离心管直至样品完全重悬。
将样本瞬时离心后置于磁力架上,待磁珠与液相完全分离,且液相澄清无色(≥ 两分钟)。保持离心管在磁力架上不动,用移液枪吸去清液。
保持离心管在磁力架上不动,打开离心管管盖,将磁珠在空气中干燥约两分钟,避免干至表面开裂。
将离心管从磁力架上取下,将磁珠重悬于 20μl 的无核酸酶水中。请吹打充分重悬磁珠。
为促进样本洗脱,将离心管置于恒温混匀仪内,在 65 °C、1,000 rpm 条件下孵育 5 分钟。
将样本置于磁力架上,待磁珠与液相完全分离,且液相澄清无色(≥ 1分钟)。
将洗脱液(~15µl)转移至一支新的1.5ml Eppendorf DNA LoBind管中。
- 将磁珠丢弃。
所提取的核酸样品即可用于后续的文库制备步骤。
如暂不使用,请将样品置于 -20 °C 保存。
4. 逆转录及PCR
材料
- 病毒样品制备:取上一步骤中提取的 10 µl 核酸
- 细菌/真菌样品制备:取上一步骤中提取的 3 µl 核酸
- 片段化反应试剂(FRM)
- 快速条形码引物(管装(RLB01-24,10 µM)或板孔装(RPB01-24,1 µM))
耗材
- 12 µM RLB RT 9N 引物(IDT - 序列:5’-TTTTTCGTGCGCCGCTTCAACNNNNNNNNN-3’)
- 12 µM TSOmG 模板转换寡核苷酸(IDT - 序列:5’-GCTAATCATTGCTTTTTCGTGCGCCGCTTCAACATmGmGmG-3’)
- 10 mM dNTPs(Fisher,10610851)
- Maxima H Minus 逆转录酶(Fisher,13233159)
- RNaseOUT(Fisher,10777019)
- LongAmp 热启动 Taq 酶 2X 预混液(NEB, M0533)
- 无核酸酶水(如 Thermo Scientific,AM9937)
- 1.5 ml Eppendorf DNA LoBind 离心管
- 0.2 ml 薄壁PCR管
仪器
- Hula混匀仪(低速旋转式混匀仪)
- 迷你离心机
- 热循环仪
- 96 孔 PCR 反应模块
- 计时器
- 盛有冰的冰桶
- P1000 移液枪和枪头
- P200 移液枪和枪头
- P100 移液枪和枪头
- P20 移液枪和枪头
- P10 移液枪和枪头
- P2 移液枪和枪头
请根据样品类型选择并遵循相应的操作步骤。
细菌/真菌样品与病毒样品的处理方法不同,请妥善记录、追踪样品,并确保采用正确的制备方法。
注意: 若同一样品分别经过细菌/真菌制备和病毒制备,在文库构建时应视为两个独立样品分别处理并添加条形码。
将下表所列试剂置于室温解冻,经迷你离心机瞬时离心后按下表方法混匀,置于冰上:
| 试剂 | 1.于室温下解冻 | 2.瞬时离心 | 3.吹打混匀 |
|---|---|---|---|
| 片段化反应试剂(FRM) | 非冰冻状态 | ✓ | ✓ |
| 快速条形码引物(管装 (RLB01-24,10 µM)或孔板装 (RPB01-24,1 µM)) | ✓ | ✓ | ✓ |
| RLB RT 9N 引物(12 µM) | ✓ | ✓ | ✓ |
| TSOmG 模板转换寡核苷酸(12 µM) | ✓ | ✓ | ✓ |
| 10 mM dNTP 溶液 | ✓ | ✓ | ✓ |
| Maxima H Minus 逆转录酶 | 非冰冻状态 | ✓ | ✓ |
| Maxima H Minus 5x RT 缓冲液 | ✓ | ✓ | ✓ |
| LongAmp Taq 2X 预混液 | ✓ | ✓ | ✓ |
| RNaseOUT | 非冰冻状态 | ✓ | ✓ |
条形码板孔仅限单次使用。使用前请确认所选孔密封完好;一旦刺穿或开启,不得再次使用。
将上一步提取的各核酸样本分别转移至一洁净的 0.2 ml 管中:
对病毒样本:
- 各样本取 10 µl 病毒核酸提取液进入下一步实验。
注意: 病毒样品的核酸浓度通常较低,常低于 Qubit HS 或其他类似荧光定量方法的检出限,因此不建议进行定量测定。建议您直接按文中推荐体积使用病毒核酸提取液。
对细菌/真菌样品:
- 各样本分别取 1 µl 细菌/真菌核酸提取液体,用 Qubit 高灵敏度(HS)试剂盒定量。
- 若测得浓度 > 1 ng/μl :请用无核酸酶水稀释至 1 ng/µl;
- 若测得浓度 ≤ 1 ng/µl 或不可定量 :请直接使用(无需稀释)。
- 随后,各样本分别取 3 µl 细菌/真菌核酸提取液(浓度已根据前一步结果调整),进入下一步实验。
根据样品类型,可并行进行相应的逆转录/酶切法片段化反应:
注意: 若同时处理两类样品,建议先处理病毒样品(因其孵育时间较长),并在病毒样品孵育期间准备细菌/真菌样品。
| 步骤 | 病毒样品制备(逆转录反应) | 对细菌/真菌样品(酶切法片段化) |
|---|---|---|
| 1. | 在一支洁净的 0.2 ml 薄壁 PCR 管中按下表配制预混液。 提示: 按所需样品数量另加一份备用配制: 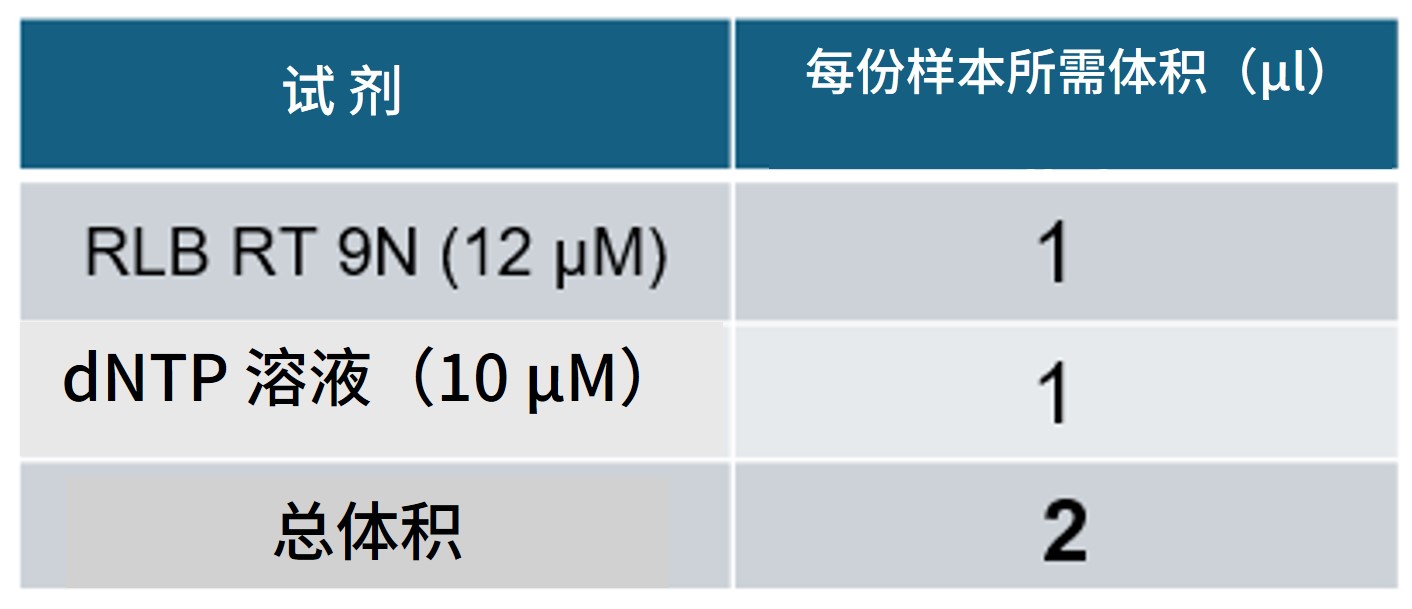 | |
| 2. | 涡旋振荡混匀预混液,然后瞬时离心。 | |
| 3. | 向每管 10 µl 病毒核酸提取液中加入 2 µl 预混液。 | |
| 4. | 65°C 下孵育 5 分钟,随后立即置于冰上。 | |
| 5. | 将样品静置于冰上两分钟。 | |
| 6. | 取一支洁净的 0.2 ml 薄壁 PCR 管,配制 Maxima H 预混液。 提示: 按所需样品数量另加一份备用配制: 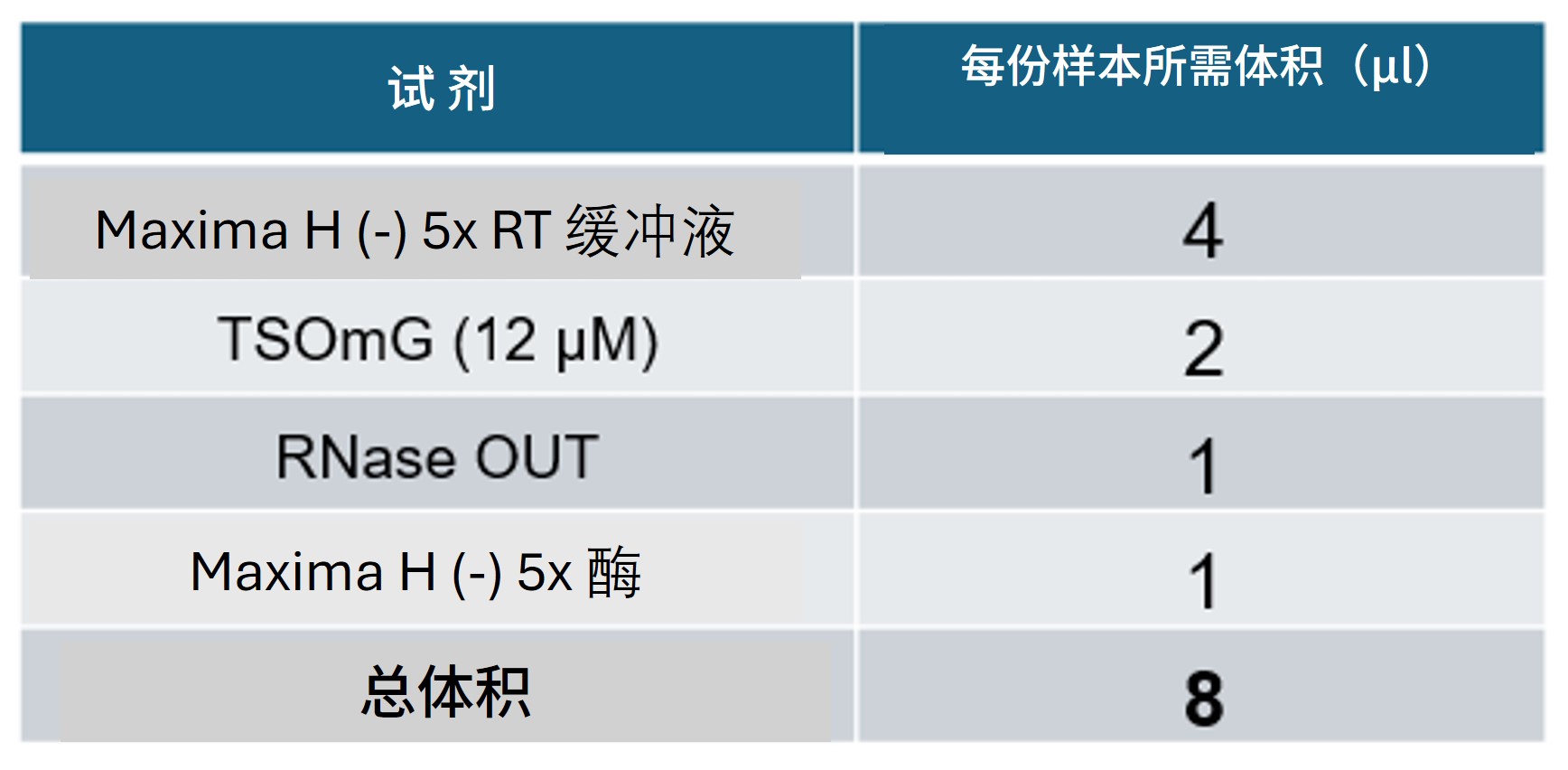 注意: 最后加入 Maxima H 酶。将预混液置于冰上保存。由于该酶为非热启动型,一旦与样品接触即开始反应,因此需在加入样品后立即进行孵育。 | |
| 7. | 向每管病毒样品中加入 8 µl Maxima H 预混液,总反应体积为 20 µl。 | |
| 8. | 将 PCR 加热模块预热至 42°C,放入样品管并按下图条件孵育: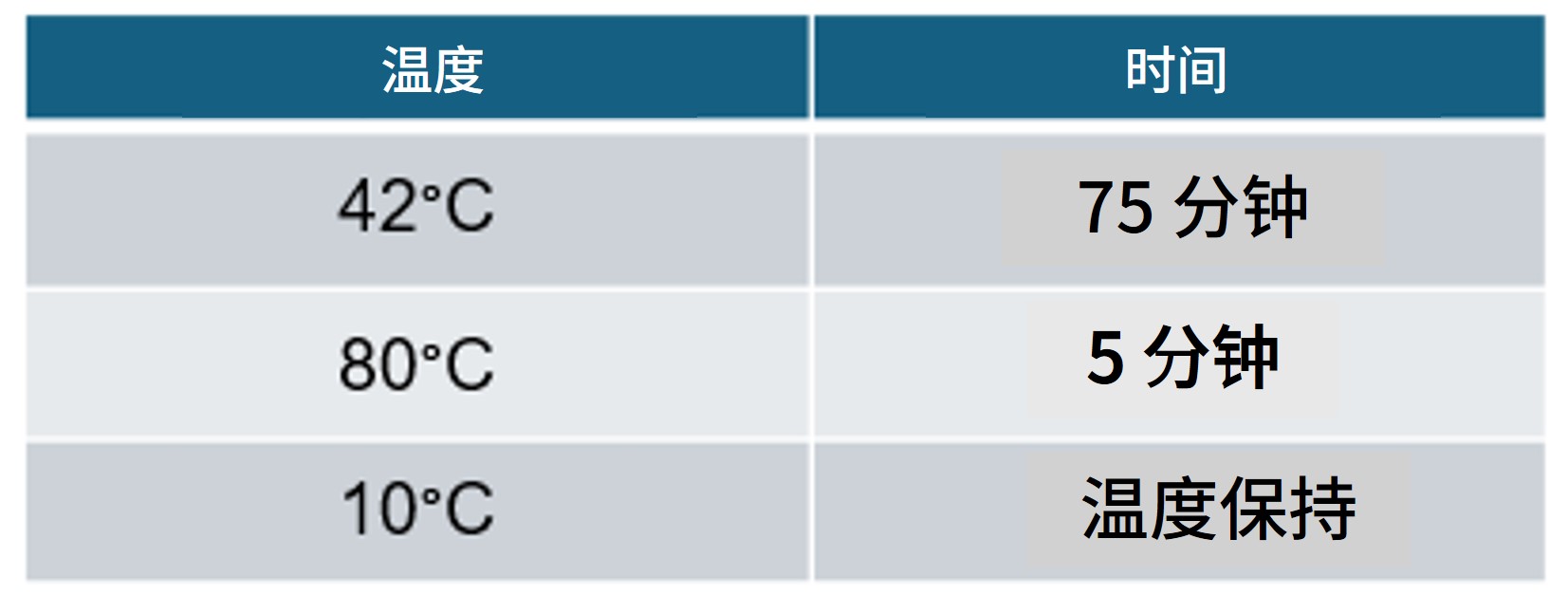 | 在病毒样品进行逆转录反应期间,可同时制备细菌/真菌样品。 |
| 9. | 向每管 3 µl 细菌/真菌 DNA 提取液中加入 1 µl FRM,轻弹 PCR 管混匀。 | |
| 10. | 将 PCR 加热模块预热至 30°C,放入样品管并按以下条件孵育: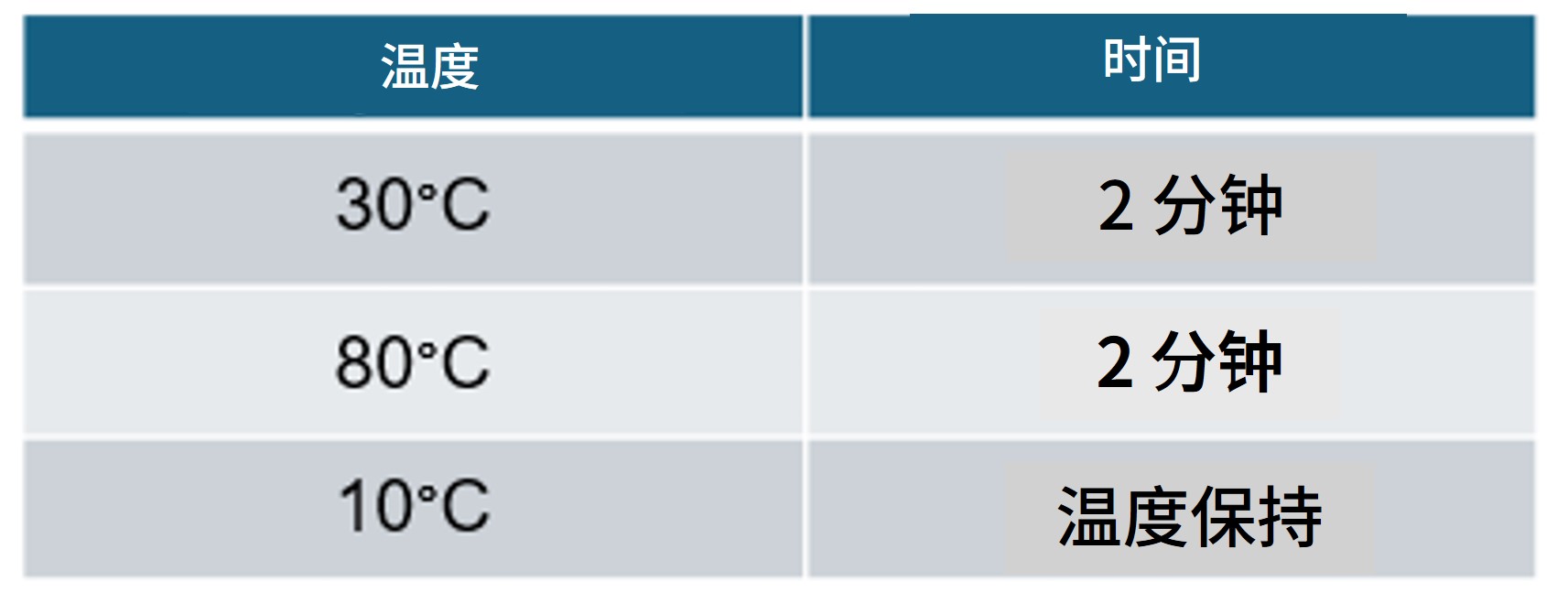 |
请确保根据所使用的 SQK-RPB114.24 试剂盒的包装形式选择正确的操作方法。
除试剂盒包装形式的变更外,我们还将条形码引物的浓度从管装形式的 10 µM 降低至孔板形式的 1 µM,以支持自动化应用,并优化试剂盒的整体使用体验。
请注意:因此变更,不同包装形式的试剂盒在 PCR 建库步骤中所需的各组分体积将有所不同,请根据实际使用的试剂盒包装形式选择对应的反应配方。
在一支洁净的 1.5 ml Eppendorf 管中按下表配置预混液:
提示: 按所需样品数量另加一份备用配制:
以孔板形式提供的 1 µM 浓度快速条形码引物
| 试剂 | 体积 |
|---|---|
| LongAmp 热启动 Taq酶 2X 预混液 | 25 µl |
| 无核酸酶水 | 11 µl |
| 总体积 | 36 µl |
使用移液枪混匀,注意避免产生气泡或泡沫。
以管装形式提供的 10 µM 浓度快速条形码引物
| 试剂 | 体积 |
|---|---|
| LongAmp 热启动 Taq酶 2X 预混液 | 25 µl |
| 无核酸酶水 | 20 µl |
| 总体积 | 45 µl |
使用移液枪混匀,注意避免产生气泡或泡沫。
注意: 本方法同样兼容非热启动型 LongAmp Taq 2X 预混液(如 NEB,M0287)。如使用该试剂替代,请按照生产商说明操作,并在冰上配制反应体系。
将预混液分装至新的 0.2 ml 薄壁 PCR 管,每个样本各一管。
向每管加入快速连接条形码引物(01–24),确保各管所用条形码引物互不相同。
注意: 为便于样本追踪,我们建议您为不同类型的样品分配不同范围的条形码编号。例如:
病毒样品用条形码 1–4,细菌/真菌样品用条形码 5–8。
以孔板形式提供的 1 µM 浓度快速条形码引物
| 试剂 | 体积 |
|---|---|
| 含有(上一步配制的)预混液的 PCR 管 | 36 µl |
| 快速连接条形码引物(01-24,1 µM) | 10 µl |
| 总体积 | 46 µl |
以管装形式提供的 10 µM 浓度快速条形码引物
| 试剂 | 体积 |
|---|---|
| 含有(上一步配制的)预混液的 PCR 管 | 45 µl |
| 快速连接条形码引物(01-24,10 µM) | 1 µl |
| 总体积 | 46 µl |
在含有预混液和快速条形码引物的反应管中,加入病毒样品(逆转录产物)或细菌/真菌样品(酶切法片段化反应产物)。
对病毒样品:
- 向反应管中加入 5 µl 逆转录病毒样品。请勿更改推荐体积, 以免影响实验结果。
| 试剂 | 体积 |
|---|---|
| 预混液 + 快速条形码引物 | 46 µl |
| 逆转录病毒样本 | 5 µl |
| 总体积 | 51 µl |
注意: 如担心样品无法达到最低摩尔浓度,建议按上述体积为同一病毒样品配制两份独立反应,PCR 结束后合并产物。请勿 更改 PCR 反应体系体积,否则可能影响反应表现并降低结果质量。
对细菌/真菌样品:
- 将全部体积的片段化反应产物加入反应管:
| 试剂 | 体积 |
|---|---|
| 预混液 + 快速条形码引物 | 46 µl |
| 经酶切片段化反应处理的细菌/真菌 DNA 样品 | ~4 µl |
| 总体积 | 50 µl |
轻弹离心管以充分混合,并瞬时离心。
按下表条件进行扩增:
| 步骤 | 温度 | 时间 | 循环数 |
|---|---|---|---|
| 预变性 | 95°C | 45 秒 | 1 |
| 变性 退火 延伸 | 95°C 56°C 65°C | 15 秒 15 秒 4 分钟 | 30 |
| 最后延伸 | 65°C | 6 分钟 | 1 |
| 保温 | 10°C | ∞ | - |
注意: PCR 总时长约 2 小时 43 分钟(具体时间可能因环境条件及设备有所差异)。
*可选:*PCR 结束后可直接在保温温度下过夜。
所得扩增产物将用于后续纯化、定量与接头连接步骤。
5. 纯化、定量与接头连接
材料
- AMPure XP 磁珠(AXP)
- 洗脱缓冲液(EB)
- 快速测序文库接头(RA)
- 接头缓冲液(ADB)
耗材
- Thermolabile 核酸外切酶 I(NEB, M0568)
- 新制备的 80% 乙醇(用无核酸酶水配制)
- 1.5 ml Eppendorf DNA LoBind 离心管
- 0.2 ml 薄壁PCR管
- Qubit™ dsDNA HS Assay(双链 DNA 高灵敏度检测)试剂盒(ThermoFisher,Q32851)
- Qubit™ 分析管(Invitrogen, Q32856)
仪器
- 热循环仪
- Hula混匀仪(低速旋转式混匀仪)
- 磁力架
- Qubit荧光计 (或用于质控检测的等效仪器)
- 计时器
- P1000 移液枪和枪头
- P200 移液枪和枪头
- P100 移液枪和枪头
- P20 移液枪和枪头
- P10 移液枪和枪头
- P2 移液枪和枪头
测序芯片质检
我们强烈建议在开始文库制备之前,对测序芯片的活性纳米孔数量进行质检,以确保其足够支持实验的顺利进行。
详情请参阅 测序芯片质检文档。
用 Qubit dsDNA HS Assay (双链DNA高灵敏度检测)试剂盒对前步所得 PCR 产物(样品管)定量。
记录各样品浓度。
注意: 样品浓度可能因起始材料差异而不同。部分样品可能低于Qubit dsDNA HS Assay (双链DNA高灵敏度检测)试剂盒的检出限,此属正常情况。
所有样品均应按下述说明继续操作。
向各样品管(PCR 产物)加入 1 µl Thermolabile Exo I,吹打混匀。
按下表条件孵育:
| 温度 | 时间 |
|---|---|
| 37°C | 10 分钟 |
| 80°C | 1 分钟 |
| 10°C | 保持 |
在一支洁净的 1.5 ml Eppendorf DNA LoBind 管中,将所有带条形码的样品按等摩尔比例混合,DNA 总量为 800 ng。
例如:若使用 10 个条码,则每个样品取 80 ng。
注意: 若样品 PCR 产物浓度过低,则取可用的最大体积进行后续步骤。
涡旋振荡以重悬 AMPure XP 磁珠(AXP)。
向混合样本中加入0.6 倍体积的 AMPure XP 磁珠(AXP)。
确保事先准确测量混合样品体积以保持比例正确。
将离心管置于Hula混匀仪(低速旋转式混匀仪)上室温孵育5分钟。
准备不少于 1 ml 新制备的 80% 乙醇(用无核酸酶水配制)。
将样品瞬时离心后置于磁力架上,待磁珠与液相分离,且液相澄清无色。保持离心管在磁力架上不动,用移液枪吸去清液。
保持试管在磁力架上不动,以 500 µl 新鲜制备的 80% 乙醇洗涤磁珠。小心不要扰动磁珠。用移液枪将乙醇吸走并弃掉。
重复上述步骤。
将离心管瞬时离心后置于磁力架上。用移液枪吸走残留的乙醇。让磁珠在空气中干燥约30秒,但不要干至表面开裂。
将离心管从磁力架上移开。将磁珠重悬于15µl洗脱缓冲液中(EB)。
室温下孵育2分钟。
将离心管置于磁力架上,直到磁珠和液相分离,且洗脱液澄清无色。
将此14 µl洗脱液转移至一支新的1.5ml Eppendorf DNA LoBind管中。
- 将含有 DNA 文库 的洗脱液转移至新的 1.5 ml Eppendorf DNA LoBind 管中
- 将磁珠丢弃
取 1μl 洗脱样品,用 Qubit dsDNA HS Assay (双链DNA高灵敏度检测)试剂盒 及 Qubit荧光计 定量。
目标回收浓度为 10-40 ng/µl。
将 11 µl 洗脱液转移至一支新的1.5ml Eppendorf DNA LoBind管中。
在一支新的 1.5 ml Eppendorf DNA LoBind 管中,按以下比例稀释快速测序文库接头(RA),并吹打混匀:
| 试剂 | 体积 |
|---|---|
| 快速测序文库接头(RA) | 1.5 μl |
| 接头缓冲液(ADB) | 3.5 μl |
| 总体积 | 5 μl |
向带有条形码的 DNA 中加入 1 µl 稀释后的快速测序文库接头(RA)。
轻弹离心管以充分混合,并瞬时离心。
室温下孵育5分钟。
构建好的文库即可用于测序芯片上样。在上样前,请将文库置于冰上或4℃条件下保存。
6. MinION 与 GridION 测序芯片的预处理及上样
材料
- 测序芯片冲洗液(FCF)
- 测序芯片系绳(FCT)
- 文库颗粒(LIB)
- 测序缓冲液(SB)
耗材
- MinION/GridION 测序芯片
- 牛血清白蛋白(BSA)(50 mg/mL)(例如 Invitrogen™ UltraPure™ BSA 50 mg/mL, AM2616)
- 1.5 ml Eppendorf DNA LoBind 离心管
仪器
- MinION 或 GridION 测序仪
- MinION/GridION 测序芯片遮光片
- P1000 移液枪和枪头
- P100 移液枪和枪头
- P20 移液枪和枪头
- P10 移液枪和枪头
请注意:本试剂盒仅兼容 R10.4.1 测序芯片(FLO-MIN114)。
从冰箱中取出测序芯片,在室温下放置 20 分钟,以便在预处理和上样时更清晰地观察到传感器阵列。
测序芯片的预处理及上样
我们建议所有新用户在首次运行测序芯片前,观看视频测序芯片的预处理及上样。
于室温下解冻测序缓冲液(SB)、文库颗粒(LIB)、测序芯片系绳(FCT)和测序芯片冲洗液(FCF)。完全解冻后,涡旋振荡混匀。然后瞬时离心,置于冰上。
为在 MinION R10.4.1 测序芯片(FLO-MIN114)上获得最优测序表现并提高测序产出,请向测序芯片预处理液中加入终浓度为 0.2 mg/ml 的牛血清白蛋白(BSA)。
注意: 我们不建议使用任何其他类型的白蛋白(例如重组人血清白蛋白)。
配制含 BSA 的芯片预处理液:将下表试剂加入至 1.5 ml 的 Eppendorf DNA LoBind 管中,在室温下颠倒并吹打混匀。
| 试剂 | 体积(每张芯片) |
|---|---|
| 测序芯片冲洗液 (FCF) | 1170 µl |
| 浓度为 50 mg/mL 的牛血清白蛋白 (BSA) | 5 µl |
| 测序芯片系绳(FCT) | 30 µl |
| 总体积 | 1205 µl |
打开 MinION 或 GridION 测序仪的盖子,将测序芯片插入金属固定夹的下方。用力向下按压预处理孔孔盖处,以确保正确的热、电接触。

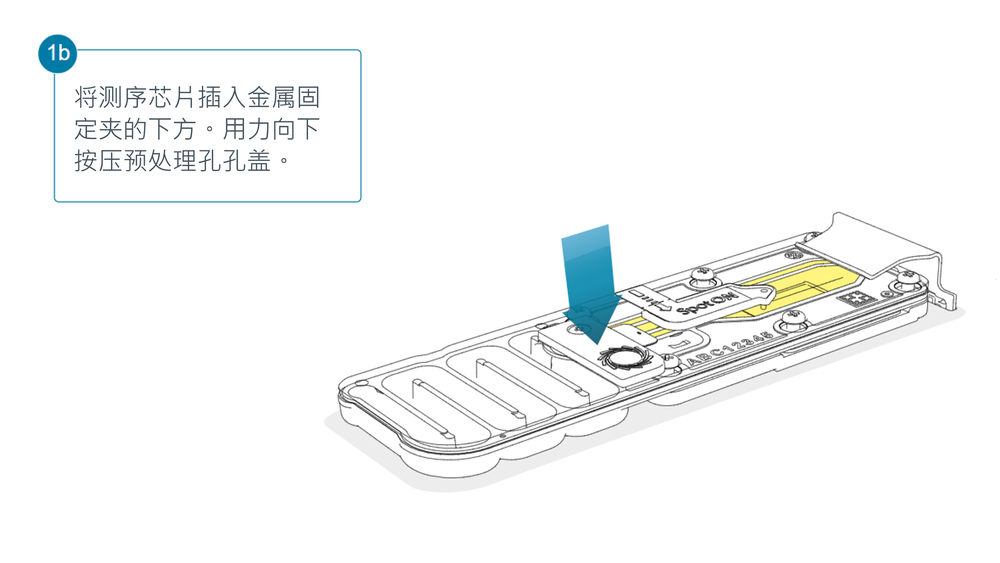
为文库上样前,完成测序芯片质检,查看可用孔数目。
如此前已对测序芯片进行过质检,则此步骤可省略。
详情请参阅 MinKNOW 实验指南中的测序芯片质检说明 。
顺时针转动测序芯片的预处理孔孔盖,使预处理孔显露出来。

小心地从测序芯片中反旋吸出缓冲液。请勿吸出超过 20-30 µl的缓冲液,并确保芯片上的纳米孔阵列一直有缓冲液覆盖。将气泡引入阵列会对纳米孔造成不可逆转地损害。
将预处理孔打开后,检查孔周围是否有小气泡。请按照以下方法,从孔中排出少量液体以清除气泡:
1.将 P1000 移液枪转至 200µl 刻度。
2.将枪头垂直插入预处理孔中。
3.反向转动移液枪量程调节转纽,直至移液枪刻度在 220-230 µl之间,或直至您看到有少量缓冲液进入移液枪枪头。
注意: 肉眼检查,确保从预处理孔到传感器阵列的缓冲液连续且无气泡。

通过预处理孔向芯片中加入 800µl 预处理液,避免引入气泡。等待5分钟。在此期间,请按照以下步骤准备用于上样的文库。

将含有文库颗粒的LIB管用移液枪吹打混匀。
LIB管内的文库颗粒分散于悬浮液中。由于颗粒沉降速度非常快,因此请在混匀颗粒后立即使用。
对于大多数测序实验,我们建议您使用文库颗粒(LIB)。但如文库较为粘稠,您可考虑使用文库溶液(LIS)。
在一支新的1.5ml Eppendorf DNA LoBind离心管内,将所有试剂按以下顺序混合:
| 试剂 | 每张测序芯片的上样体积 |
|---|---|
| 测序缓冲液(SB) | 37.5 µl |
| 文库颗粒 (LIB),临用前混匀 | 25.5 µl |
| DNA 文库 | 12 µl |
| 总体积 | 75 µl |
完成测序芯片的预处理:
- 轻轻地翻起SpotON上样孔盖,使SpotON上样孔显露出来。

- 通过预处理孔(而 非 SpotON加样孔)向芯片中加入200µl预处理液,避免引入气泡。

临上样前,用移液枪轻轻吹打混匀制备好的文库。
通过 SpotON 加样孔向芯片中逐滴加入 75µl 制备好的文库。确保液滴流入孔内后,再加下一滴。

轻轻合上 SpotON 加样孔孔盖,确保塞头塞入加样孔内。合上预处理孔盖。


为获得最佳测序产出,在文库样本上样后,请立即在测序芯片上安装遮光片。
我们建议在文库加样至测序芯片后(包括芯片清洗并重新加样时),将遮光片保留在测序芯片上。一旦文库从测序芯片中吸出,即可取下遮光片。
按下述步骤安装测序芯片遮光片:
1.小心将遮光片的前沿(平端)与金属固定夹的边沿对齐。 注意: 请勿将遮光片强行压到固定夹下方。
2.将遮光片轻轻盖在测序芯片上。遮光片的 SpotON 加样孔孔盖缺口应与芯片上的 SpotON 加样孔孔盖接合,遮盖住整个测序芯片的前部。

MinION测序芯片的遮光片并非固定在测序芯片上,因此当为芯片加装遮光片后,请小心操作。
合上测序设备上盖,在 MinKNOW 上设置测序实验。
将测序芯片插入 MinION Mk1D 测序仪后,仪器上盖会覆盖于芯片上方,芯片四周可能留有一条小缝隙。此为正常现象,不影响设备性能。
请参阅此 常见问题解答 ,了解有关测序仪上盖的更多信息。

7. 数据采集和碱基识别
我们不建议在同一设备上同时进行测序和数据分析。
为确保设备计算性能满足测序和/或分析需求, 强烈建议避免同时运行这两项任务 。
请确保测序实验完成后再启动分析。数据分析应在测序结束后进行。
同样,若设备正在进行数据分析,请避免启动新的测序任务。
如何开始测序
MinKNOW 软件负责测序设备的控制、数据采集和实时碱基识别。请确保已在计算机或设备上安装 MinKNOW。有关测序实验的详细设置说明,请参阅 MinKNOW 实验指南。
我们建议您按照下文设置碱基识别和条码拆分参数,其余参数可保持默认值。
在 MinKNOW 中设置快速宏基因组测序
为加快实验进程并简化分析,我们建议您在测序运行过程中使用高精准(HAC)碱基识别模型进行实时碱基识别。
MinKNOW 推荐设置如下:
测序芯片位置
测序芯片位置 :[用户定义]
实验名称 :[用户定义]
测序芯片类型 :FLO-MIN114
样本 ID: [用户定义]
试剂盒
选择试剂盒: 快速PCR条形码测序试剂盒(SQK-RPB114)
实验配置
测序和分析
碱基识别 :开 [默认]
修饰碱基 :关
模型 :高精准碱基识别(HAC) [默认]
条码拆分 :开 [默认]
去条码 :关 [默认]
双端条形码: 关 [默认]
自定义选择条形码: 关 [默认]
比对 :关 [默认]
适应性采样 :关 [默认]
进阶选项
活性通道选择 :开 [默认]
孔扫描间隔时间 :1.5 [默认]
预留孔 :开 [默认]
数据目标
运行限制条件 :[用户定义]*
* 实际测序时间取决于数据需求:如需快速获取信息,可在测序约 30 分钟后开始分析;如需最大化数据产出,可连续测序最长 72 小时。
输出
输出格式
.POD5 :开 [默认]
.FASTQ : 开 [默认]
.BAM :开
过滤 :开 [默认]
质量值 :9 [默认]
最短读长 :200 bp [默认]
8. 下游分析
我们不建议在同一设备上同时进行测序与数据分析。
为确保设备计算性能满足测序和/或分析需求, 强烈建议避免同时运行这两项任务 。
请确保测序实验完成后再启动分析。数据分析应在测序结束后进行。
同样,若设备正在进行数据分析,请避免启动新的测序任务。
下游分析
我们建议使用 EPI2ME 进行下游分析。EPI2ME 为一款桌面软件,可运行 Nextflow 工作流程,帮助用户高效开展生物信息学分析。平台内的分析流程由长读长测序领域的专家精心开发维护。
安装方法详见 EPI2ME 安装指南 ,使用说明请参考 EPI2ME 快速入门指南。
测序软件生成的数据可通过 wf-metagenomics 工作流程进行高效分析。该流程基于 Nextflow 构建,是一条生物信息学处理管线,能够对样本中各物种进行鉴定与丰度估算。结合推荐数据库,可准确识别人类、真菌、细菌、病毒、古菌及原生生物序列。
我们建议您始终使用最新版本的工作流程,并参考 EPI2ME wf-metagenomics 文档页面获取有关该工作流程的使用方法及结果说明的更多信息。
注意
- 该工作流程亦可通过命令行运行,但此方式仅建议有经验的用户使用。请访问 GitHub 上的wf-metagenomics 页面 ,获取更多信息及最新版本。 若使用命令行运行,建议采用以下设置,以确保流程发挥最佳性能:
--kraken2_confidence 0.01 --database_set PlusPF-8 --store_dir /path/to/database/download/directory/
- /path/to/database/download/directory/ 为占位符,请根据用户系统替换为实际数据库路径。
您可在 GitHub 获取用于验证 wf-metagenomics 工作流程的测试数据。
测试数据可于以下存储库中获取:wf-metagenomics 测试数据.
在 EPI2ME 中运行 wf-metagenomics
您可在 EPI2ME 应用程序的 Workflows(工作流程)界面中,通过 “Available Workflows”(可用工作流程)页面选择并安装所需流程。
已安装的工作流程可在 “Installed”(已安装)页面查看。
您可使用工作流程自带的小型测试数据集验证安装是否成功:
1.启动 EPI2ME 应用程序
2.选择 View workflows (查看工作流程)
3.选择 wf-metagenomics 工作流程
4.选择 Use demo data (使用演示数据)
5.启动工作流程
6.流程运行完成后,可在 “Report(报告)” 页查看结果。该工作流程将生成交互式 HTML 报告。
运行工作流程
采用此“双路径宏基因组学”实验指南,运行 wf-metagenomics 工作流程时的推荐参数设置如下:
1.启动 EPI2ME 应用程序
2.选择 View workflows (查看工作流程)
3.选择 wf-metagenomics 工作流程
4.选择 Run this workflow (运行此工作流程)。
5.选择 本地运行或云端运行(如适用)
6.在 “Input Options(输入选项)” 中,指定输入数据(FASTQ 或 BAM 格式)。
7.在 “样本选项(Sample Options)” 中上传 CSV 格式的样本列表。
我们建议您为每个条形码指定一个别名,以区分样本及类型(例如:sample_A_viral,sample_A_bacterial)。
8.在 "Reference Options"(参考序列选项)中, 选择 PlusPF-8 database ,以确保工作流程能够识别古菌、细菌、病毒、人类及真菌类群。
9.在 "Kraken2 Options"(Kraken2 选项)中, 将 Confidence score threshold (置信度阈值)设置为 0.01
10.点击 Launch workflow (启动工作流程)
11.流程运行完成后,您可在 “Report” (报告)页查看结果。该流程将生成一份交互式 HTML 报告。
注意: 未特别说明的参数建议保持默认设置。
可选项: 如有需要,可在工作流程设置中调整本地 CPU 和内存的资源分配。
9. 测序芯片的重复利用及回收
材料
- 测序芯片清洗剂盒(EXP-WSH004)
完成测序实验后,如您希望再次使用测序芯片,请按照“测序芯片清洗试剂盒实验指南”进行操作,并将清洗后的芯片置于 +2 至 +8℃ 保存。
您可在纳米孔社区获取测序芯片清洗试剂盒实验指南。
我们建议您在停止测序实验后尽快清洗测序芯片。如若无法实现,请将芯片留在测序设备上,于下一日清洗。
或者,请按照回收程序将测序芯片返还至 Oxford Nanopore。
您可在 此处找到回收测序芯片的说明。
如果您遇到问题或对测序实验有疑问,请参阅本实验指南在线版本中的“疑难解答指南”一节。
10. DNA/RNA提取和文库制备过程中可能出现的问题
以下表格列出了提取和文库制备过程中的常见问题,以及可能的原因和解决方法。
我们还在 Nanopore 社区的Support板块提供了常见问题解答(FAQ)。
如果以下方案仍无法解决您的问题,请通过电邮(support@nanoporetech.com)或 纳米孔社区的在线支持(LiveChat)联系我们。
低质量样本
| 现象 | 可能原因 | 措施及备注 |
|---|---|---|
| 低纯度DNA(Nanodrop测定的DNA吸光度比值260/280<1.8,260/230 <2.0-2.2) | 用户所使用的DNA提取方法未能达到所需纯度 | 您可在 污染物专题技术文档中查看污染物对后续文库制备和测序实验的影响。请尝试其它不会导致污染物残留的 提取方法 。 请考虑将样品再次用磁珠纯化。 |
| RNA完整值低 (RNA完整值(RIN)<9.5,或 rRNA 在电泳凝胶上的条带呈弥散状) | RNA在提取过程中降解 | 请尝试其它RNA 提取方法.您可在RNA完整值 文档中查看更多有关RNA完整值(RIN)的介绍。更多信息,请参阅 DNA/RNA 操作 页面。 |
| RNA的片段长度短于预期 | RNA在提取过程中降解 | 请尝试其它 RNA 提取方法。您可在RNA完整值 文档中查看更多有关RNA完整值(RIN)的介绍。更多信息,请参阅 DNA/RNA 操作 页面。 |
经AMPure磁珠纯化后的DNA回收率低
| 现象 | 可能原因 | 措施及备注 |
|---|---|---|
| 低回收率 | AMPure磁珠量与样品量的比例低于预期,导致DNA因未被捕获而丢失 | 1.AMPure 磁珠沉降速度较快,因此在将磁珠加入样品前,请务必充分重悬混匀。 2.当AMPure磁珠量与样品量的比值低于0.4:1时,所有的DNA片段都会在纯化过程中丢失。 |
| 低回收率 | DNA片段短于预期 | AMPure磁珠量与样品量的比值越低,针对短片段的筛选就越严格。每次实验时,请先使用琼脂糖凝胶(或其他凝胶电泳方法)确定起始DNA的长度,据此计算出合适的AMPure磁珠用量。! SPRI cleanup |
| 末端修复后的DNA回收率低 | 清洗步骤所用乙醇的浓度低于70% | 当乙醇浓度低于70%时,DNA会从磁珠上洗脱下来。请确保使用正确浓度的乙醇。请确保使用正确浓度的乙醇。 |
11. 使用快速测序试剂盒时,测序过程中可能出现的问题
以下表格列出了提取和文库制备过程中的常见问题,以及可能的原因和解决方法。
我们还在 Nanopore 社区的Support板块提供了常见问题解答(FAQ)。
如果以下方案仍无法解决您的问题,请通过电邮(support@nanoporetech.com)或 纳米孔社区的在线支持(LiveChat)联系我们。
MinKNOW Mux 扫描在测序起始时报告的活性孔数少于芯片质检时报告的活性孔数
| 现象 | 可能原因 | 措施及备注 |
|---|---|---|
| MinKNOW Mux 扫描在测序起始时报告的活性孔数少于芯片质检时报告的活性孔数 | 纳米孔阵列中引入了气泡 | 在对通过质控的芯片进行预处理之前,请务必排出预处理孔附近的气泡。否则,气泡会进入纳米孔阵列对其造成不可逆转地损害。视频中演示了避免引入气泡的最佳操作方法。 |
| MinKNOW Mux 扫描在测序起始时报告的活性孔数少于芯片质检时报告的活性孔数 | 测序芯片没有正确插入测序仪 | 停止测序,将芯片从测序仪中取出,再重新插入测序仪内。请确保测序芯片牢固嵌入测序仪中,并已到达目标温度。如用户使用的是GridION/PromethION测序仪,也可尝试将芯片插入仪器的其它芯片槽进行测序。 |
| MinKNOW Mux 扫描在测序起始时报告的活性孔数少于芯片质检时报告的活性孔数 | 文库中残留的污染物对纳米孔造成损害或堵塞 | 在测序芯片质检阶段,我们用芯片储存缓冲液中的质控DNA分子来评估活性纳米孔的数量。而在测序开始时,我们使用DNA文库本身来评估活性纳米孔的数量。因此,活性纳米孔的数量在这两次评估中会有约10%的浮动。如测序开始时报告的孔数明显降低,则可能是由于文库中的污染物对膜结构造成了损坏或将纳米孔堵塞。用户可能需要使用其它的DNA/RNA提取或纯化方法,以提高起始核酸的纯度。您可在 污染物专题技术文档中查看污染物对测序实验的影响。请尝试其它不会导致污染物残留的 提取方法。 |
MinKNOW脚本失败
| 现象 | 可能原因 | 措施及备注 |
|---|---|---|
| MinKNOW显示 "Script failed”(脚本失败) | 重启计算机及MinKNOW。如问题仍未得到解决,请收集 MinKNOW日志文件并联系我们的技术支持。如您没有其他可用的测序设备,我们建议您先将装有文库的测序芯片置于4°C 储存,并联系我们的技术支持团队获取进一步储存上的建议。 |
纳米孔利用率低于40%
| 现象 | 可能原因 | 措施及备注 |
|---|---|---|
| 纳米孔利用率<40% | 测序芯片中的文库量不够 | 请确保您按照相应实验指南,向 MinION/GridION 测序芯片中加入正确浓度的优质文库。如需确认所需的上样浓度,请参阅建库实验指南。请在上样前对文库进行定量,并使用Promega Biomath Calculator等工具中的“dsDNA:µg to pmol”功能来计算 DNA 分子的摩尔量。 |
| 纳米孔利用率接近0 | 使用快速测序试剂盒 V14/快速条形码测序试剂盒 V14,但测序接头并未与 DNA 成功连接 | 请务必严格遵循实验方案,使用准确的体积并保持正确的孵育温度。您可通过制备Lambda对照文库来检验试剂的可用性。 |
| 纳米孔利用率接近0 | 测序芯片中无系绳 | 系绳(FCT 管)随测序芯片预处理液加至芯片。请确保在制备预处理液时,将测序芯片系绳(FCT)加入测序芯片冲洗液(FCF)中。 |
读长短于预期
大量纳米孔处于不可用状态
| 现象 | 可能原因 | 措施及备注 |
|---|---|---|
大量纳米孔处于不可用状态 (在通道面板和纳米孔活动状态图上以蓝色表示) 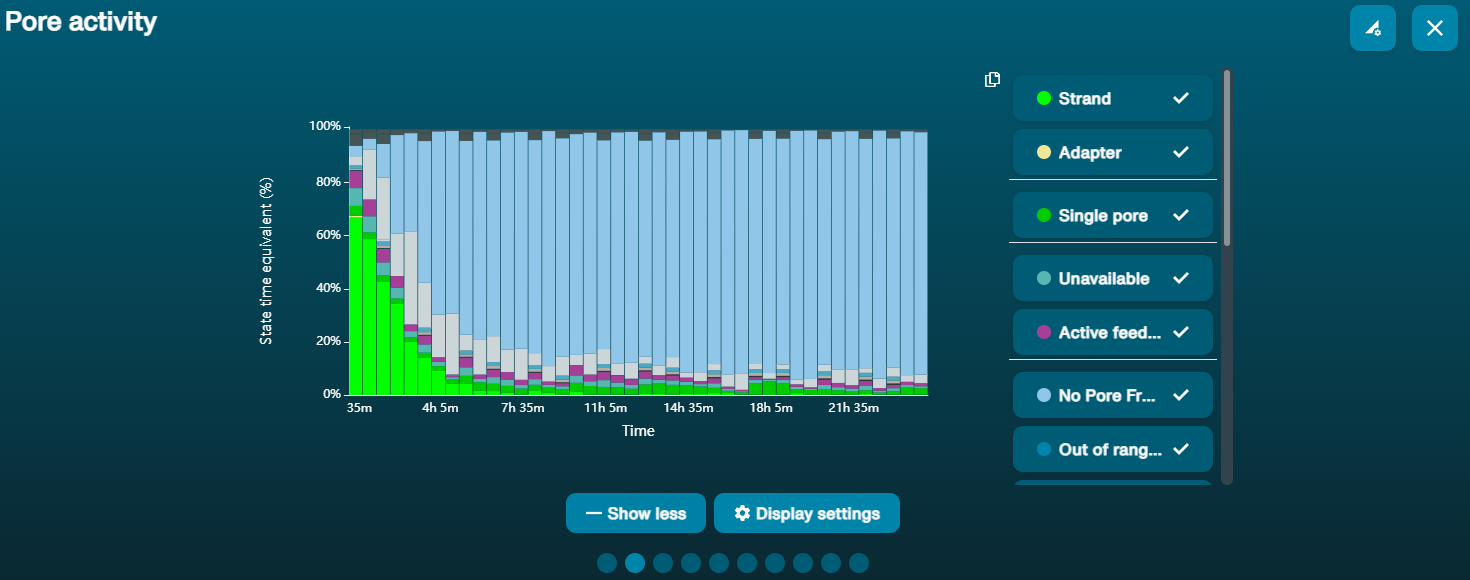 上方的纳米孔活动状态图显示:状态为不可用的纳米孔的比例随着测序进程而不断增加。 上方的纳米孔活动状态图显示:状态为不可用的纳米孔的比例随着测序进程而不断增加。 | 样本中含有污染物 | 使用MinKNOW中的“Unblocking”(疏通)功能,可对一些污染物进行清除。如疏通成功,纳米孔的状态会变为"测序孔"(sequencing pore)。若疏通后,状态为不可用的纳米孔的比例仍然很高甚至增加: 1.用户可使用 测序芯片冲洗试剂盒 (EXP-WSH004)进行核酸酶冲洗 操作,或 2.使用PCR扩增目标片段,以稀释可能导致问题的污染物。 |
大量纳米孔处于“失活”(Inactive)状态
| 现象 | 可能原因 | 措施及备注 |
|---|---|---|
| 大量纳米孔处于失活状态(在通道面板和纳米孔活动状态图上以浅蓝色表示。膜结构或纳米孔遭受不可逆转地损伤 | 测序芯片中引入了气泡 | 芯片预处理和文库上样过程中引入的气泡会对纳米孔带来不可逆转地损害。请观看 测序芯片的预处理及上样 视频了解最佳操作方法 |
| 大量纳米孔处于失活/不可用状态 | 存在与DNA共纯化的化合物 | 已知的化合物包括通常与植物基因组 DNA 相关的多糖等。请参考植物叶片DNA提取方法. 2.使用 QIAGEN PowerClean Pro 试剂盒进行纯化。 3.利用QIAGEN REPLI-g试剂盒对原始gDNA样本进行全基因组扩增。 |
| 大量纳米孔处于失活/不可用状态 | 样本中含有污染物 | 您可在Contaminants 中查看污染物对测序实验的影响。请尝试其它不会导致污染物残留的提取方法。 |
温度波动
| 现象 | 可能原因 | 措施及备注 |
|---|---|---|
| 温度波动 | 测序芯片和仪器接触不良 | 检查芯片背面的金属板是否有热垫覆盖。重新插入测序芯片,用力向下按压,以确保芯片的连接器引脚与测序仪牢固接触。如问题仍未得到解决,请联系我们的技术支持。 |
未能达到目标温度
| 现象 | 可能原因 | 措施及备注 |
|---|---|---|
| MinKNOW显示“未能达到目标温度” | 测序仪所处环境低于标准室温,或通风不良(以致芯片过热) | MinKNOW会限定测序芯片达到目标温度的时间。当超过限定时间后,系统会显示出错信息,但测序实验仍会继续。值得注意的是,在错误温度下测序可能会导致通量和数据质量(Q值)的降低。请调整测序仪的摆放位置,确保将其置于室温下、通风良好的环境中,再在MinKNOW中重启进程。有关 MinION 温度控制的更多信息,请点击 此链接查看。 |







